Alteraciones neuromusculares asociadas a la COVID-19. Revisión de la literatura científica
Neuromuscular Alterations Associated with COVID-19. A Scientific Literature Review
Eulalia Maria Amador-Rodero , Priscila Mishelle Bartolo Gómez, Fátima del Carmen Carrasco Ferrer, Nancy Paola Ochoa Castillo, Leslie Piedad Montealegre Esmeral, Roberto Carlos Rebolledo Cobos
Resumen
Introducción: La pandemia por la COVID-19 ha traído consecuencias a corto, mediano y largo plazo sobre la calidad de vida de los afectados. Entre las complicaciones se encuentran aquellas relacionadas con la afectación del sistema nervioso y las estructuras involucradas en el movimiento corporal, con secuelas que pueden ser transitorias y/o definitivas, y requieren rehabilitación.
Objetivo: Identificar las alteraciones neuromusculares que afectan el movimiento corporal, asociadas a la COVID-19.
Material y métodos: Se hizo una búsqueda de trabajos observacionales publicados en las bases de datos SCOPUS, PubMed, EBSCO y Nature entre enero de 2020 y junio de 2022 bajo metodología PRISMA, para dar respuesta a la pregunta PICO: ¿cuáles son las alteraciones neuromusculares que potencialmente pueden afectar el movimiento, asociadas a la COVID-19? Los filtros establecidos fueron tipo de estudio, idioma, edad, disponibilidad y fechas de publicación. Los términos MesH fueron SARS-Cov-2, COVID-19, Long Covid, Motor Activity Neuromuscular Diseases, Neurological Disorders, Guillain-Barré Syndrome, Myelitis Transverse, Stroke, Patient, Peripheral Nervous System Diseases. La calidad metodológica se evaluó según STROBE y el nivel de evidencia se estableció según CEBM.
Resultados: En la primera búsqueda se identificaron 645 artículos. Posteriormente se descartaron 637 por filtros, títulos, resúmenes duplicados, calidad metodológica y nivel de evidencia. Así, quedaron seleccionados 8 para la presente revisión, en los cuales se identificaron alteraciones neuromusculares de origen central y periférico, como mialgias, fatiga, polineuroradiculopatías, inflamación del SNC, entre otras, con manifestaciones clínicas que afectan el movimiento.
Conclusión: La COVID-19 es una enfermedad multisistémica que puede afectar el sistema nervioso con síntomas de alteraciones neuromusculares que comprometen el movimiento corporal.
Palabras clave
SARS-Cov-2, COVID-19, Long Covid, Desorden de la actividad neuromuscular, desordenes neurológicos, Sindrome de Guillain Barre, Mielitis Transversa, Ataque, Paciente, Desorden del sistema nervioso periférico.
Abstract
Introduction: The COVID-19 pandemic has brought short, medium, and long-term consequences on the quality of life of those affected. Among the complications are those related to the involvement of the nervous system and the structures involved in body movement, with sequelae that may be transitory and/or definitive, and require rehabilitation.
Objective: Identify the neuromuscular alterations that affect body movement, associated with COVID-19.
Material and methods: A search was made for observational works published in the SCOPUS, PubMed, EBSCO, and Nature databases between January 2020 and June 2022 under the PRISMA methodology, to answer the PICO question: what are the neuromuscular alterations that can potentially affect movement, associated with COVID-19? The established filters were type of study, language, age, availability, publication dates. The MeSH terms were SARS-Cov-2, COVID-19, Long Covid, Motor Activity Neuromuscular Diseases, Neurological Disorders, Guillain-Barré Syndrome, Myelitis Transverse, Stroke, Patient, Peripheral Nervous System Diseases. The methodological quality was evaluated according to STROBE and the level of evidence was established according to CEBM.
Results: In the first search, 645 articles were identified. 637 were discarded by filters, titles, duplicate abstracts, methodological quality, and level of evidence. There were 8 articles selected for the present review, in which neuromuscular alterations of central and peripheral origin were identified, such as myalgias, fatigue, polyneuroradiculopathies, CNS inflammation, among others, with clinical manifestations that affect movement.
Conclusion: COVID-19 is a multisystemic disease that can affect the nervous system with symptoms of neuromuscular alterations that compromise body movement.
Keywords
SARS-Cov-2, COVID-19, Long Covid, Motor activity neuromuscular diseases, neurological disorders, Guillain-Barré Syndrome, Myelitis transverse, Stroke, patient, Peripheral nervous system diseases.
Introducción
El nuevo coronavirus, descubierto en China e identificado como SARS-CoV-2, es un virus beta coronavirus de tipo zoonótico [1], que tiene una morbimortalidad a nivel mundial sin precedentes [2]. La Organización Panamericana de la Salud (OPS) [3] reportó el 1 de julio de 2022 un total de casos acumulados en la región de las Américas de 163,260,535, de los cuales 2,762,900 fueron muertes acumuladas y 160,497,635 fue el total de casos recuperados. Un estudio del 24 de noviembre del 2021 al 27 de febrero del 2022 sobre la variante Omicrón del SARS-CoV a nivel mundial encontró un incremento de casos del 41,50% [4]. Uno de los países con alta mortalidad en América Latina es México, con 325,793 defunciones en Julio de 2022 [5]. En Colombia, el Instituto Nacional de Salud reportó para la misma fecha 6,175,181 de casos confirmados, de los cuales 140,070 fueron defunciones y 5,984,546 fue el total de casos recuperados [6].
Los estudios indican que la enfermedad originada por SARS-CoV-2, llamada COVID-19 por la Organización Mundial de la salud (OMS), es causante de una tormenta de citocinas con estado posinflamatorio, lo que da lugar a complicaciones vasculares y de hipercoagulabilidad, generando mayor riesgo de sufrir enfermedad cerebrovascular (ECV), afectación de estructuras involucradas en el control motor con signos y síntomas de disfunción para el control, regulación del movimiento y complicaciones neuromusculares que afectan la motricidad y ponen en riesgo la vida de quien la padece [7]. Algunos autores evaluaron neurológicamente a pacientes ingresados en unidades de cuidados intensivos (UCI) por la COVID-19 y encontraron patología neuromuscular (16,66%), patología cerebrovascular (13,33%) y encefalopatías/encefalitis (13,33%) [8]. Otros autores además observaron que la estancia en UCI da lugar a una mayor restricción del movimiento, debido a periodos prolongados en cama, lo que representa un riesgo adicional de pérdida de la masa muscular, especialmente en las personas mayores [9].
También se han identificado alteraciones emergentes asociadas a la COVID-19 con afección motora y gran potencial mortal, dentro de los cuales se encuentra el síndrome de Guillain-Barré, enfermedad neurológica autoinmune [10], debido a la formación de autoanticuerpos que dirigen su actividad hacia las vainas de mielina [11]. Por otro lado, se ha observado una rápida desmielinización, dando lugar a una mielitis transversa [12], los cuales generalmente cursan en el periodo agudo de la enfermedad. Hay otros síntomas duraderos en paciente que se recuperan de una fase aguda y se denominan síndrome post-agudo de COVID-19 o secuelas post-agudas de la infección por SARS-CoV-2 (PASC) o long/Covid, en donde también se presentan varios síntomas y manifestaciones neuromusculares [13] con alteraciones motoras.
Todos los pacientes con COVID-19 están potencialmente en riesgo de desarrollar estas enfermedades, cuyos mecanismos fisiopatológicos se exacerban por las respuestas autoinmunes e hiperinflamatorias de la enfermedad, dejando secuelas susceptibles de intervención desde la rehabilitación. A pesar del impacto sobre la calidad de vida de los pacientes, en la búsqueda de información para la presente revisión no se encontraron estudios que agrupen o consoliden las alteraciones neuromusculares, sus secuelas o sus abordajes desde la rehabilitación. Tener conciencia de ello es fundamental para que los equipos puedan detectar de forma temprana los casos complicados. Por ello se considera que el presente estudio puede robustecer la evidencia que ayuda a salvar vidas y a disminuir la discapacidad. La presente revisión tuvo como objetivo identificar las alteraciones neuromusculares asociadas a la COVID-19 en pacientes adultos mayores de 18 años de edad a través de una revisión de literatura científica.
Materiales y métodos
Se hizo una revisión de literatura científica para dar respuesta a la pregunta PICO: ¿Cuáles son las alteraciones neuromusculares asociadas a la COVID-19?
Criterios de selección y estrategia de búsqueda
Se realizó una búsqueda exhaustiva de artículos entre el 27 de junio de 2022 y el 25 de Julio de 2022 en las bases de datos SCOPUS, PubMed, EBSCO y Nature. Los límites establecidos fueron: publicaciones de estudios observacionales en full texto, escritos en español, inglés y portugués, publicados los últimos 10 años, con énfasis en 2020-2022.
Se utilizaron los términos MesH: “SARS-Cov-2”, “COVID-19”, “Long Covid”, “Motor activity neuromuscular diseases”, “Neurological disorders”, “Guillain-Barré Syndrome”, “Myelitis transverse”, “Stroke, patient” y “Peripheral nervous system diseases”. Se combinaron con los operadores boleanos AND or NOT y se introdujeron en las bases de datos seleccionadas.
Criterios de inclusión
Se incluyeron estudios observacionales referidos a pacientes con COVID-19 y/o Long Covid, cuya enfermedad cursó o cursaba con alteraciones del sistema nervioso central y/o neuromuscular, masculinos y femeninos, mayores de 18 años, hospitalizados y no hospitalizados.
Criterios de exclusión
Fueron excluidos aquellos estudios de pacientes que cursaron o cursaban COVID-19 sin complicaciones neurológicas y/o neuromusculares; aquellos estudios que incluían pacientes con COVID-19 con enfermedades y/o alteraciones neuromusculares preexistentes que podían inducir a sesgos en los resultados.
Extracción de datos
La búsqueda la hicieron los investigadores por separado y la selección se hizo mediante consenso. Después de aplicar los filtros y excluir títulos y resúmenes, duplicidad, idioma, fecha de publicación y no cumplir criterios de inclusión, a los resultantes se les hizo la evaluación de la calidad metodológica mediante Strengthening the Reporting of Observational studies in Epidemiology (STROBE por siglas en inglés), aplicándosele como cumplimiento mínimo del 75% de los ítems (contiene 22 items). A los preseleccionados se les valoró el nivel de evidencia con el protocolo del Centre for Evidence-Based Medicine de Oxford (CEBM por sus siglas en inglés), escogiéndose aquellos estudios con alto nivel de evidencia y grados de recomendación (ver Tabla 1). Se procedió a extraer la información que permitió dar respuesta a la pregunta PICO.
Tabla 1. Características de los estudios incluidos en la revisión sistemática.
| Título del artículo | Autores | Participaciones (PICOS) | Intervención (PICOS) | Comparación (PICOS) | Desenlace (PICOS) | Diseño del estudio (PICOS) |
|---|---|---|---|---|---|---|
| Guillain-Barré Syndrome Related and Unrelated to COVID-19: Clinical Follow-Up in the COVID-19 Era [8] | Masuccio FG, Tipa V, Invernizzi M, Solaro C. | N = 11 | Examinación de pacientes con GBS asociado a COVID-19 utilizando el índice de Barthel y GBS-Escala de discapacidad. | Pacientes con C-GBS y pacientes con NC-GBS. | El 55,55% de los pacientes con GBS asociado a COVID-19 tuvieron un mejor resultado clínico ya que recuperaron la marcha de manera autónoma. | Observacional cohorte |
| Long COVID: rheumatologic/musculoskeletal symptoms in hospitalized COVID-19 survivors at 3 and 6 months [13] | Karaarslan F, Güneri FD, Kardeş S. | N = 300 | Descripción de síntomas reumáticos y musculoesqueléticos en sobrevivientes de COVID-19. | No aplica | A los 3 meses, el 89,0% de los supervivientes tenía al menos un síntoma, el 74,6% tenía al menos un síntoma reumático y musculoesquelético (mialgias, artralgias, lumbalgias) y el 82,1% tenía al menos otro síntoma de COVID-19. A los 6 meses, el 59,6% de los supervivientes tenía al menos un síntoma, el 43,2% tenía al menos un síntoma reumático y musculoesquelético (mialgias, artralgias, lumbalgias) y el 51,2% tenía al menos otro síntoma de COVID-19. | Observacional cohorte |
| Clinical and Electrophysiological Outcome Measures of Patients With Post-Infectious Neurological Syndromes Related to COVID-19 Treated With Intensive Neurorehabilitation [14] | Avenali M, Martinelli D, Todisco M, Canavero I, Valentino F, Micieli G, et al. | N = 5 pacientes | Ilustrar la recuperación neurofisiológica y funcional en pacientes con síndromes neurológicos para-infección y post-infección (PINS) después de COVID-19 | No aplica | Se recuperó la función y la independencia en 1 paciente con Polirradiculoneuropatía desmielinizante inflamatoria aguda (AIDP) asociada a COVID-19 y de forma moderada en dos de los pacientes que cursaban con AIDP y neuropatía axonal sensorial y motora aguda. 1 paciente con mielitis mostró control motor central prolongado y otro tuvo una recuperación con persistencia de debilidad muscular de miembros inferiores. | Observacional cohorte |
| Predictors of long covid 19 syndrome [15] | Mady AF, Abdelfattah RA, Kamel FMM, Abdel Naiem ASM, AbdelGhany WM, Abdelaziz AO. | N = 164 | Evaluar los síntomas que persisten después de la etapa aguda de la enfermedad en una cohorte de pacientes con sospecha o confirmación de COVID 19 y definir los predictores de síndrome de COVID prolongado. | Pacientes con previa confirmación o alta sospecha de COVID-19 atendidos en El-Minia University Chest Hospital | Los síntomas neuromusculares informados con mayor frecuencia fueron fatiga crónica y neuropatía (15,2 %); vértigo y cefalea (9,1%), las artralgias y las mialgias (6,1%). | Cohorte retrospectivo |
| Intracortical GABAergic dysfunction in patients with fatigue and dysexecutive syndrome after COVID-19 [16] | Versace V, Sebastianelli L, Ferrazzoli D, Romanello R, Ortelli P, Saltuari L, et al. | N = 12 pacientes | Aplicar estimulación transcranial magnética (TMS) para explorar la actividad de los circuitos intracorticales inhibitorios en la corteza primaria (M1) en pacientes con fatiga y disfunción después de COVID-19 con síntomas neurológicos. | Pacientes con complicaciones neurológicas después de COVID-19 vs pacientes sanos (control) | Pacientes PostCOVID-19 mostraron fatiga con el Fatigue Rating Scale con score (8.1 ± 1.7) y score patológico en el Frontal Assessment Battery (12.2 ± 0.7). La estimulación transcraneal magnética mostró reducción de la inhibición cortical a intervalos cortos (p < 0.001 en 2ms y p < 0.01 en 3 ms) y disrupción de la inhibición cortical a intervalos largos (p = 0.008 en 50 ms y p < 0.001 en 100 ms) a comparación de los sanos | Observacional cohorte |
| Subclinical myopathic changes in COVID-19 [17] | Villa D, Ardolino G, Borellini L, Cogiamanian F, Vergari M, Savojardo V, Peyvandi F, Barbieri S. | N = 12 pacientes | Evaluar la relación entre SARS-Cov-2 y la función neuromuscular primaria | No aplica | Se mostró cambios miopáticos con electromiografía de aguja (6/12) prominentes en los músculos trapecio (50%), iliopsoas (33%) y deltoides (8%) todos asintomáticos en síntomas musculares. No existieron diferencias significativas en los laboratorios en los grupos. | Cohorte |
| Evolving phenotypes of non-hospitalized patients that indicate long COVID [18] | Estiri H, Strasser ZH, Brat GA, Semenov YR, Aaron JR, Agapito G, et al. | N = 96,025 | Identificación precisa de los fenotipos de secuelas post-agudas de COVID-19 | Pacientes vivos y no hospitalizados. que se sometieron a pruebas de reacción en cadena de la polimerasa con transcriptasa inversa por SARS-CoV-2 | Se identificaron 33 fenotipos, entre ellos fatiga crónica y debilidad muscular como secuelas post-agudas de COVID-19 (PASC) más frecuentes en pacientes no hospitalizados. | Cohorte Retrospectivo |
| Myopathic changes in patients with long-term fatigue after COVID-19 [19] | Agergaard J, Leth S, Pedersen TH, Harbo T, Blicher JU, Karlsson P, et al. | N = 20 pacientes | Investigar el nervio periférico y la función electrofisiológica del músculo en pacientes con síntomas neuromusculares persistentes después de COVID-19 | Pacientes con Long Covid con síntomas neuromusculares persistentes vs control de pacientes sanos del mismo sexo y edad | El potencial de unidad motora se redujo en el bíceps braquial, vasto medial y tibial anterior en comparación con el control (p < 0.0001); la fatiga física y mialgia fue más común en pacientes con electromiografía comparado con el grupo control (p < 0.05) | Cohorte observacional |
Nota. N = número de muestra.
Resultados
Resultados de la búsqueda
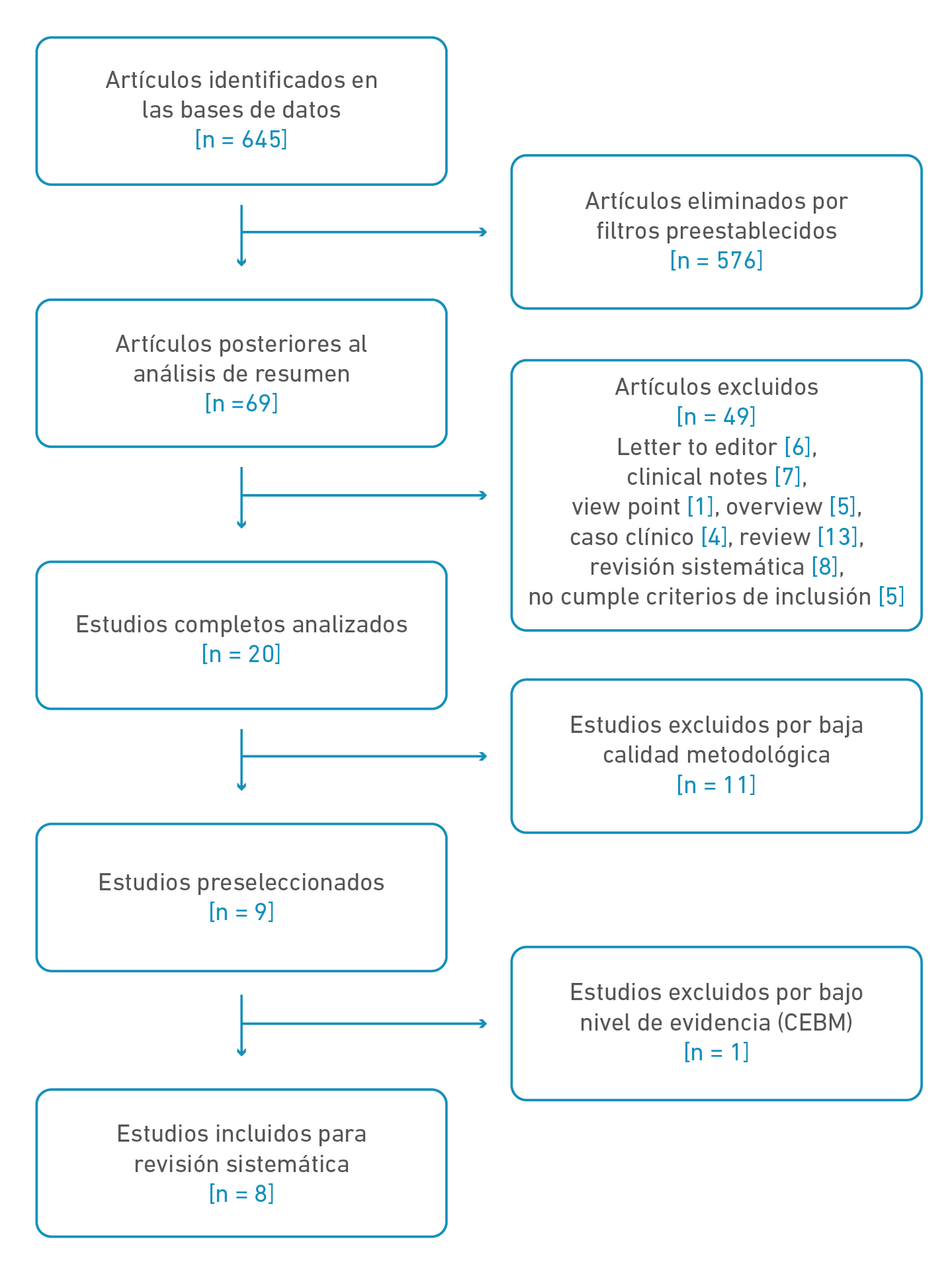
Al finalizar la selección de la primera búsqueda se obtuvo un total de 645 artículos (PubMed, 74; SCOPUS, 185; EBSCO, 76; Nature, 310). Después de pasar por los diferentes filtros quedaron para análisis 69 artículos (PubMed, 23; SCOPUS, 20; EBSCO, 22; Nature, 4). De estos se excluyeron 49 por no cumplir criterios, quedando 20, a los cuales se les hizo evaluación de la calidad metodológica, quedando 9 preseleccionados. Luego de valorar el nivel de evidencia y grado de recomendación se excluyó 1 y fueron seleccionado 8 para la presente revisión (Figura 1).
Figura 1. Diagrama de flujo, búsqueda, clasificación y selección de artículos.
Características de los estudios
En la Tabla 1 se indican las características de cada uno de los estudios [8,13-19], es decir, su identificación con la referencia, los datos de los participantes, el tipo de intervención, la comparación (de estar o no presente), el desenlace y el tipo de estudio. Estos parámetros fueron evaluados con la guía del acrónimo PICOS. Se incluyeron estudios desarrollados en países como Estados Unidos, Italia, Turquía, Egipto y Suiza.
Riesgo de sesgo
En cuanto al riesgo de sesgo, se encontró que los métodos diferían para cada estudio, lo que podía inducir a sesgos. Sin embargo, cada autor hacía explicito los mecanismos.
Análisis de heterogeneidad
Se encontró que los estudios analizados diferían en cuanto a la selección de la población y los instrumentos de medición.
Síntesis de resultados
La presente revisión permitió identificar que, asociado a la COVID-19, se presentan alteraciones neuromusculares de origen central y/o periférico transitorias y/o definitivas que afectan el movimiento, y por consiguiente la funcionalidad y funcionamiento de quienes lo padecen [8,13-19]. Al respecto:
El objetivo de Masuccio et al. [8] fue establecer el desenlace de pacientes con GBS asociado a COVID-19, utilizando el índice de Barthel y discapacidad de 11 pacientes. En esta cohorte se detectó una prevalencia superior a la esperada de neuropatía axonal motora aguda. El grupo de GBS relacionado con COVID-19 no tuvo ninguna complicación. Después de una media de 10,11 meses (DE = 4,46 meses), el 55,55% de los pacientes recuperaron la marcha autónoma.
El objetivo de Karaarslan et al. [13] fue documentar las características relacionadas con la gravedad, tipo y ubicación de síntomas reumáticos y musculoesqueléticos en 300 sobrevivientes de COVID-19 con edades de 18 a 70 años. Encontraron a los tres meses que el 74,6% tenía al menos un síntoma reumático y musculoesquelético (mialgias, artralgias, lumbalgias); y a los 6 meses, el 43,2% tenía al menos un síntoma reumático y musculoesquelético (mialgias, artralgias, lumbalgias). Estas manifestaciones obedecen especialmente a los cambios a nivel musculoesquelético manifiestos por atrofia muscular, y las limitaciones para los movimientos fueron en parte producidos por la inactividad física como consecuencia de la enfermedad [8].
El objetivo de Avenali et al. [14] fue ilustrar la recuperación neurofisiológica y funcional en 5 pacientes con síndromes neurológicos para-infección y post-infección (PINS) después de COVID-19, a los cuales se les hizo seguimiento durante seis meses. El grupo de pacientes cursaron con inflamación del sistema nervioso central y periférico como respuesta a la infección por el SarsCov2, manifiestas por polineuroradiculopatia, neuropatía axonal motora y sensorial aguda, mielitis transversa. Concluyeron que los pacientes con afectaciones periféricas tuvieron peor pronóstico que los de nivel central.
El objetivo de Mady et al. [15] fue evaluar los síntomas que persistían después de la etapa aguda de la enfermedad en 164 pacientes con más de tres meses de evolución de la enfermedad. Identificaron fatiga crónica y neuropatía (15,2%), disnea crónica en 9,8% mayoritariamente en casos severos, vértigo y cefalea en 9,1%, síntomas musculoesqueléticos en 6,1% y lesiones cutáneas en 3,7%.
El objetivo de Versace et al. [16] fue explorar la actividad de los principales circuitos intracorticales inhibitorios dentro de la corteza motora primaria (M1) en una muestra de 12 pacientes que se quejaban de fatiga y presentaban disfunción ejecutiva después de la resolución de COVID-19 con manifestaciones neurológicas. Observaron cambios en las corrientes sinápticas corticales que pueden desarrollar síntomas persistentes aun después de la enfermedad, tales como reducción en la inhibición de la corteza motora primaria (M1), como disrupción de los circuitos intracorticales GABAaérgicos (encargados de suministrar las señales para la salida funcionales del cerebro), mediado por inhibición intracortical de intervalo corto a través de estimulación transcraneal magnética (p < 0.001), con síntomas motores como la fatiga y algunas alteraciones en las funciones ejecutivas.
El objetivo de Villa et al. [17] fue evaluar el alcance de la afectación neuromuscular primaria en la infección por SarsCov2 en un grupo de 70 pacientes entre 18 a 70 años, 12 de los cuales no tenían enfermedad grave en tres semanas de seguimiento. Encontraron cambios miopáticos con electromiografía de aguja (6/12) prominentes en los músculos trapecio (50%), iliopsoas (33%) y deltoides (8%); todos asintomáticos en síntomas musculares.
El objetivo de Estiri et al. [18] fue identificar los fenotipos de secuelas post-agudas de COVID-19 en 96,025 sujetos. Se identificaron 33 fenotipos entre diferentes cohortes de edad/género o ventanas de tiempo que se asociaron positivamente con una infección anterior por SARS-CoV. Entre estos fenotipos, dolor torácico (OR 1,27, IC 95% [1,09-1,48]), síndrome de fatiga crónica (OR 2,60, IC 95 % [1,22-2,10]), dificultad para respirar (OR 1,41, IC 95 % [1,22-1,64]), neumonía (OR 1,66, IC 95 % [ 1.28-2.16]). Además, la diabetes mellitus tipo 2 (OR 1.41, 95% IC [1.22-1.64]) es uno de los indicadores más significativos de una infección pasada por COVID-19. Por otro lado, se encontraron más fenotipos nuevos con mayor confianza entre las cohortes menores de 65 años.
El objetivo de Agergaard et al. [19] fue investigar el nervio periférico y la función electrofisiológica del músculo en 20 pacientes con síntomas neuromusculares persistentes después de COVID-19. Los resultados incluyeron la reducción del potencial de unidad motora en el bíceps braquial, vasto medial y tibial anterior, en comparación con el control (p < 0.0001); la fatiga física y mialgia, comparada con el grupo control, fue más común en pacientes con electromiografía (p < 0.05).
Los problemas neurológicos que afectan la actividad motora tuvieron en algunos estudios un peor diagnóstico y pronóstico en los pacientes hospitalizados en UCI. Frontera et al. [20] reportaron que el 91% de los pacientes tuvo al menos un resultado anormal en seis meses y aquellos con complicaciones neurológicas durante la hospitalización no podían cumplir con las actividades de la vida diaria (CI 0.29-.74, p=0.01) y solamente el 41% pudo regresar a su trabajo de forma normal en ese periodo, comparado al 64% de los pacientes sin complicaciones neurológicas.
Discusión
En la presente revisión se identificaron alteraciones neuromusculares en pacientes con COVID-19 como una complicación derivada de la misma, aunque con diferentes mecanismos de acción; afectación con signos y síntomas de diferentes estructuras del sistema nervioso central y periférico, lo que incide en el control y regulación del movimiento. Entre las manifestaciones se hallaron enfermedades que tienen su propia fisiopatogenia exacerbada por el estado infeccioso e hiperinflamatorio.
Las alteraciones neuromusculares pueden obedecer a la penetración del SARS-CoV-2 en las neuronas, lo cual puede alterar sus procesos celulares, como disfunción mitocondrial y daño en los lisosomas, al inducir un aumento de las especies reactivas de oxígeno (ROS), el mal plegamiento/agregación de proteínas y, en última instancia, la muerte celular [11,21]. Esto hace que el virus SARS-CoV-2 no sea estrictamente neurotrópico, a diferencia de otros coronavirus encontrados previamente [22,23].
Sin embargo, se ha asociado la infección de COVID-19 a una variedad de complicaciones neuromusculares que van desde síntomas inespecíficos y moderados, como cefalea, mialgia e hiposmia, hasta síntomas graves, como enfermedad cerebrovascular, encefalitis, encefalopatía, esclerosis múltiple, trastornos de movilidad y ataxia, neuropatía periférica, enfermedad de la unión neuromuscular y trastornos musculares [23,24], la mayoría identificadas en el presente estudio, mismas que pueden ocurrir durante la fase agua de la infección o como manifestaciones postvirales [6].
En una de las afectaciones de origen central se identificó la ECV. Algunos autores como Wirth et al. [25] observaron que estos ocurrieron en sujetos más jóvenes con enfermedad de moderada a grave y en el 1-5 % de los pacientes hospitalizados con COVID-19, debido a que el nuevo coronavirus induce un estado de hipercoagulabilidad, causando niveles elevados de dímero D y fibrinógeno. Otro posible mecanismo está representado por la disfunción endotelial, como consecuencia de la depleción de la enzima convertidora de angiotensina al infectar directamente las células endoteliales; la angiotensina II no podría ser contrarrestada, produciendo un estado proinflamatorio, vasoconstricción, y promoviendo una lesión tisular también en el cerebro y sus vasos [25,26]. Estos pacientes pueden presentar alteraciones en el control motor, como hemiplejia y ataxia, incluso un nivel reducido de conciencia [27].
Las encefalopatías han sido reportadas en un tercio de los de los pacientes hospitalizados, especialmente en adultos. Puede deberse a enfermedad pulmonar significativa o compromiso multiorgánico, las anomalías hipóxicas o metabólicas [22].
La disnea con alteración mecánica respiratoria se debe a una sobreestimulación del músculo esquelético. Esta situación metabólica modificada provoca un impulso respiratorio excesivo con restricción de las funciones pulmonares [28]. Pueden desarrollar síntomas inespecíficos, como dolor de cabeza, alteración de la conciencia, alteraciones visuales, convulsiones, pérdida de memoria, velocidad de procesamiento lenta, delirio o incluso coma [27,29]. Recientemente esta condición ha tenido una importante recuperación, gracias a la fisioterapia torácica y la neurorrehabilitación [30,31].
En la mielitis trasversa (TM) por infección del virus SARS-CoV-2, el paciente presenta parestesias, debilidad flácida aguda y lumbalgia [32]. Puede progresar rápidamente a paraplejía con anestesia total por debajo de cierto nivel de la médula espinal [28]. Fisiológicamente, este virus tiene propiedades neuroinvasivas y neurotrópicas, haciendo que la diseminación, ataque y desmielinización neuronal en el SNC se precipite [12]. La gravedad de la enfermedad está relacionada con la edad avanzada, las enfermedades respiratorias y cardiovasculares, la hipertensión, la diabetes y los pacientes con inmunodeficiencia [20].
También se encontró como patología asociada a la COVID-19 el síndrome de Guillain-Barré (GBS), que es el resultado del mimetismo celular molecular y formación de anticuerpos que se dirigen a los proteoglucanos encontrados en las vainas de mielina [11], el cual se caracteriza por manifestar una debilidad simétrica ascendente progresiva, arreflexia y pérdida sensorial [10]. El GBS post infeccioso asociado a COVID-19 se debe a una respuesta inmune exagerada, con marcadores inflamatorios y citocinas proinflamatorias elevadas. En este tipo de GBS se presentan las mismas manifestaciones clínicas [7]. Para diagnosticar GBS se deben destacar signos motores alterados, daño axonal y disociación de albumina citológica en el líquido cefalorraquídeo [32-33].
La intervención temprana en las complicaciones neurológicas como GBS y la mielitis puede ocasionar un mejor pronóstico. Aun así, puede existir un considerable daño axonal que dificulte una recuperación rápida, unido a la inmovilidad en algunos pacientes que puede alterar los resultados en el potencial motor cuantitativo [16,21].
El GBS y la TM pueden coexistir en un paciente Long-Covid. Este es llamado síndrome de superposición de GBS/TM, que puede incluir elementos de GBS, como lo son parálisis flácida, debilidad motora, hiporreflexia o arreflexia, y en el TM: signos piramidales y disfunción a nivel sensorial [32].
El síndrome de fatiga crónica complica de manera marcada complicación a aquellos pacientes que han desarrollado Long-Covid, sobre todo el sexo femenino [14,7] siendo el exponente más relevante por la ausencia de recuperación [33]. Así, obedece a la presencia de citocinas postinflamatorias, como el interferón (IFN-γ), que al atravesar la barrera hematoencefálica, dirigen su acción sobre el hipotálamo, generando la fatiga profunda e incapacitante, mialgia a largo plazo, reducción de la actividad diaria y malestar posterior a esfuerzos [13,21]. Algunos estudios indican una tasa de prevalencia del síndrome de fatiga crónica del 16,8%. Los síntomas más frecuentemente identificados son fatiga general postesfuerzo, dolor de cabeza, insomnio, disosmia, disgeusia, mareos, entre otras [34].
Otros hallazgos involucran directamente al músculo esquelético, muchas veces asociados a la disminución en la actividad física (AF), lo que afecta directamente la fisiología músculoesquelética. Al respecto, algunos hallazgos sugieren que la tormenta de citocinas, junto con la expresión de coagulopatías y la alteración de la actividad de los macrófagos, puede ser la razón del daño a las células musculares [19,35]. También han sugerido que las miopatías y alteraciones sensitivas en algunos pacientes pueden deberse al estrés mitocondrial y microtrombos que pueden expresarse hasta 40 días después de COVID-19 [36].
Son múltiples las complicaciones respiratorias y sistemas, entre ellas las del sistema neuromuscular, que puede padecer un paciente con SarsCov2, lo que sin duda alguna representa un deterioro de su calidad de vida. La rehabilitación siempre será una oportunidad para la recuperación del paciente [37] y su reincorporación a la vida cotidiana.
Conclusiones
Existe evidencia para comprender el papel de la COVID-19 en el desarrollo de las alteraciones neuromusculares; la presencia o no de estas puede deberse a ciertos factores de riesgos: gravedad de infección, el tiempo que el paciente estuvo en UCI y la oportuna identificación de la sintomatología. Sin embargo, los estudios están limitados por un campo que solo abarca los síntomas respiratorios, dejando inconclusos los mecanismos fisiopatológicos del sistema musculoesquelético y el sistema nervioso central y periférico. Es necesario que los investigadores enfoquen su atención en invertir conocimiento para responder a las necesidades en cuanto a la identificación, el diagnóstico temprano, pronóstico, tratamiento, junto con rehabilitación adecuada y oportuna. Todo para minimizar las consecuencias en la calidad de vida de los pacientes afectados. Se recomienda hacer trabajos de tipo prospectivos para obtener información relacionada con el tema.
Referencias
1. Delafontaine A, Ditcharles S, Hussein T, Hoffschir M, Plantefève G, Michon D. Physiotherapy and COVID-19: A major public health role to short, medium and long terms in the patient’s rehabilitation process. Kinesitherapie. 2020;20(223):11-18. doi: https://doi.org/10.1016/j.kine.2020.05.005
2. Nalbandian A, Sehgal K, Gupta A, Madhavan MV, McGroder C, Stevens JS, et al. Post-acute COVID-19 syndrome. Nat Med [Internet]. 2021;27(4):601-15. doi: https://doi.org/10.1038/s41591-021-01283-z
3. Organización Panamericana de la Salud (OPS). Enfermedad por el Coronavirus (COVID-19) [Internet]. Paho.org. [citado el 5 de julio de 2022]. Disponible en:
4. Mora D. Impacto de la Variante Ómicron Del Sars-Cov-2 en el mundo. RADA [Internet]. 26 de julio de 2022 [citado 9 de diciembre de 2022];5(1):353-70. Disponible en: https://revistas.utn.ac.cr/index.php/arje/article/view/527
5. Agarwal A, Pinho M, Raj K, Yu FF, Bathla G, Achilleos M, et al. Neurological emergencies associated with COVID-19: stroke and beyond. Emerg Radiol [Internet]. 2020;27(6):747-54. doi: https://doi.org/10.1007/s10140-020-01837-7
6. Abenza-Abildúa MJ, Ramírez-Prieto MT, Moreno-Zabaleta R, Arenas-Valls N, Salvador-Maya MA, Algarra-Lucas C, et al. Neurological complications in critical patients with COVID-19. Neurología (English Edition) [Internet]. 2020 Nov;35(9):621-7. doi: http://dx.doi.org/10.1016/j.nrleng.2020.07.012
7. Sagarra-Romero L, Viñas-Barros A. COVID-19: Short and Long-Term Effects of Hospitalization on Muscular Weakness in the Elderly. International Journal of Environmental Research and Public Health [Internet]. 2020 Nov 24;17(23):8715. doi: http://dx.doi.org/10.3390/ijerph17238715
8. Masuccio FG, Tipa V, Invernizzi M, Solaro C. Guillain-Barré Syndrome Related and Unrelated to COVID-19: Clinical Follow-Up in the COVID-19 Era. Phys Ther. 2022 Jun 3;102(6):pzac049. doi: https://doi.org/10.1093/ptj/pzac049
9. Kirwan, R., McCullough, D., Butler, T. et al. Sarcopenia during COVID-19 lockdown restrictions: long-term health effects of short-term muscle loss. GeroScience. 2020;42:1547-1578. doi: https://doi.org/10.1007/s11357-020-00272-3
10. Fumery T, Baudar C, Ossemann M, London F. Longitudinally extensive transverse myelitis following acute COVID-19 infection. Mult Scler Relat Disord. 2021 Feb;48:102723. doi: https://doi.org/10.1016/j.msard.2020.102723
11. Shimohata T. Neuro‐COVID‐19. Clinical and Experimental Neuroimmunology [Internet]. 2021 Sep 29;13(1):17-23. doi: http://dx.doi.org/10.1111/cen3.12676
12. Wong T., Weitzer D. Long COVID and Myalgic Encephalomyelitis/Chronic Fatigue Syndrome (ME/CFS)-A Systemic Review and Comparison of Clinical Presentation and Symptomatology. Medicina MDPI. 2021;54:418. doi: https://doi.org/10.3390/medicina57050418
13. Karaarslan F, Güneri FD, Kardeş S. Long COVID: rheumatologic/musculoskeletal symptoms in hospitalized COVID-19 survivors at 3 and 6 months. Clinical Rheumatology [Internet]. 2021 Oct 29;41(1):289-96. doi: http://dx.doi.org/10.1007/s10067-021-05942-x
14. Avenali M, Martinelli D, Todisco M, Canavero I, Valentino F, Micieli G, et al. Clinical and Electrophysiological Outcome Measures of Patients With Post-Infectious Neurological Syndromes Related to COVID-19 Treated With Intensive Neurorehabilitation. Front Neurol. 2021;12. doi: https://doi.org/10.3389/fneur.2021.643713
15. Mady AF, Abdelfattah RA, Kamel FMM, Abdel Naiem ASM, AbdelGhany WM, Abdelaziz AO. Predictors of long covid 19 syndrome. Egypt J Hosp Med [Internet]. 2021;85(2):3604-8. doi: https://doi.org/10.21608/ejhm.2021.201970
16. Versace V, Sebastianelli L, Ferrazzoli D, Romanello R, Ortelli P, Saltuari L, et al. Intracortical GABAergic dysfunction in patients with fatigue and dysexecutive syndrome after COVID-19. Clin Neurophysiol. 2021;132(5):1138-1143. doi: https://doi.org/10.1016/j.clinph.2021.03.001
17. Villa D, Ardolino G, Borellini L, Cogiamanian F, Vergari M, Savojardo V, Peyvandi F, Barbieri S. Subclinical myopathic changes in COVID-19. Neurol Sci. 2021;42(10):3973-3979. doi: https://doi.org/10.1007/s10072-021-05469-8
18. Estiri H, Strasser ZH, Brat GA, Semenov YR, Aaron JR, Agapito G, et al. Evolving phenotypes of non-hospitalized patients that indicate long COVID. BMC Medicine [Internet]. 2021 Sep 27;19(1). doi: http://dx.doi.org/10.1186/s12916-021-02115-0
19. Agergaard J, Leth S, Pedersen TH, Harbo T, Blicher JU, Karlsson P, et al. Myopathic changes in patients with long-term fatigue after COVID-19. Clinical Neurophysiology [Internet]. 2021 Aug;132(8):1974-81. doi: http://dx.doi.org/10.1016/j.clinph.2021.04.009
20. Frontera JA, Yang D, Lewis A, Patel P, Medicherla C, Arena V, et al. A prospective study of long-term outcomes among hospitalized COVID-19 patients with and without neurological complications. Journal of the Neurological Sciences [Internet]. 2021 Jul;426:117486. doi: http://dx.doi.org/10.1016/j.jns.2021.117486
21. Abboud H, Abboud FZ, Kharbouch H, Arkha Y, El Abbadi N, El Ouahabi A. COVID-19 and SARS-Cov-2 Infection: Pathophysiology and Clinical Effects on the Nervous System. World Neurosurgery [Internet]. 2020 Aug;140:49-53. doi: http://dx.doi.org/10.1016/j.wneu.2020.05.193
22. Vidale S. Risk Factors, and Clinical and Etiological Characteristics of Ischemic Strokes in COVID-19-Infected Patients: A Systematic Review of Literature. Cerebrovascular Diseases [Internet]. 2021;50(4):371-4. doi: http://dx.doi.org/10.1159/000514267
23. Haffke M, Freitag H, Rudolf G, Seifert M, Doehner W, Scherbakov N, et al. Endothelial dysfunction and altered endothelial biomarkers in patients with post-COVID-19 syndrome and chronic fatigue syndrome (ME/CFS). Journal of Translational Medicine [Internet]. 2022 Mar 22;20(1). doi: http://dx.doi.org/10.1186/s12967-022-03346-2
24. Fotuhi M, Mian A, Meysami S, Raji CA. Neurobiology of COVID-19. Journal of Alzheimer’s Disease [Internet]. 2020 Jun 30;76(1):3-19. Disponible en: http://dx.doi.org/10.3233/jad-200581
25. Wirth KJ, Scheibenbogen C. Dyspnea in Post-COVID Syndrome following Mild Acute COVID-19 Infections: Potential Causes and Consequences for a Therapeutic Approach. Medicina [Internet]. 2022 Mar 12;58(3):419. doi: http://dx.doi.org/10.3390/medicina58030419
26. Harapan BN, Yoo HJ. Neurological symptoms, manifestations, and complications associated with severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) and coronavirus disease 19 (COVID-19). Journal of Neurology [Internet]. 2021 Jan 23;268:3059-3071. doi: http://dx.doi.org/10.1007/s00415-021-10406-y
27. Raveendran AV, Jayadevan R, Sashidharan S. Long COVID: An overview. Diabetes & Metabolic Syndrome: Clinical Research & Reviews [Internet]. 2021 May;15(3):869-75. doi: http://dx.doi.org/10.1016/j.dsx.2021.04.007
28. Ahmad SJ, Feigen CM, Vazquez JP, Kobets AJ, Altschul DJ. Neurological Sequelae of COVID-19. Journal of Integrative Neuroscience [Internet]. 2022 Apr 6;21(3):77. doi: http://dx.doi.org/10.31083/j.jin2103077
29. Alrubaye R, Bondugula V, Baleguli V, Chofor R. A possible Guillain-Barré syndrome/transverse myelitis overlap syndrome after recent COVID-19. BMJ Case Reports [Internet]. 2022 Feb;15(2):e246967. doi: http://dx.doi.org/10.1136/bcr-2021-246967
30. Raahimi MM, Kane A, Moore CE, Alareed AW. Late onset of Guillain-Barré syndrome following SARS-CoV-2 infection: part of ‘long COVID-19 syndrome’? BMJ Case Reports [Internet]. 2021 Jan;14(1):e240178. doi: http://dx.doi.org/10.1136/bcr-2020-240178
31. Vallejo Serna R, Cantor González JF, Arce Gálvez L. Síndrome de Guillain-Barré asociado a COVID-19: diagnóstico, tratamiento y rehabilitación. Neurology Perspectives [Internet]. 2021 Jan;1(1):104-6. doi: http://dx.doi.org/10.1016/j.neurop.2021.03.003
32. Sundar Shrestha D, Love R. Long COVID Patient Symptoms and its Evaluation and Management. Journal of Nepal Medical Association [Internet]. 2021 Aug 12;59(240). doi: http://dx.doi.org/10.31729/jnma.6355
33. Bax F, Lettieri C, Marini A, Pellitteri G, Surcinelli A, Valente M, et al. Clinical and neurophysiological characterization of muscular weakness in severe COVID-19. Neurological Sciences [Internet]. 2021 Mar 23;42(6):2173-8. doi: http://dx.doi.org/10.1007/s10072-021-05110-8
34. Tokumasu K, Honda H, Sunada N, Sakurada Y, Matsuda Y, Yamamoto K, et al. Clinical Characteristics of Myalgic Encephalomyelitis/Chronic Fatigue Syndrome (ME/CFS) Diagnosed in Patients with Long COVID. Medicina [Internet]. 2022 Jun 25;58(7):850. Available from: http://dx.doi.org/10.3390/medicina58070850
35. Chakravarty N, Senthilnathan T, Paiola S, Gyani P, Castillo Cario S, Urena E, et al. Neurological pathophysiology of SARS‐CoV‐2 and pandemic potential RNA viruses: a comparative analysis. FEBS Letters [Internet]. 2021 Nov 22;595(23):2854-71. doi: http://dx.doi.org/10.1002/1873-3468.14227
36. Nath A, Smith B. Neurological issues during COVID-19: An overview. Neuroscience Letters [Internet]. 2021 Jan;742:135533. doi: http://dx.doi.org/10.1016/j.neulet.2020.135533
37. Almanza-Díaz Y, Carmona-Ferrer B, Sabater-Hernández H. Consideraciones sobre rehabilitación pos-COVID-19. Revista Cubana de Medicina Física y Rehabilitación [revista en Internet]. 2022 [citado 24 Oct 2022];14(3). Disponible en: http://www.revrehabilitacion.sld.cu/index.php/reh/article/view/784